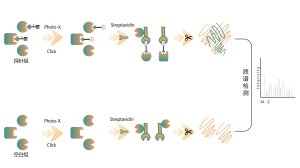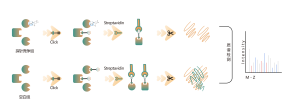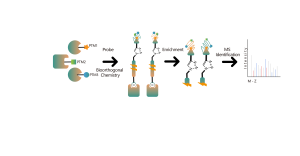Produkter
Små molekyl-proteininteraktioner
Proteiner, som direkta deltagare och utförare av livsaktiviteter, representerar avgörande mål för sjukdomsterapi. Läkemedel med små molekyler (organiska föreningar typiskt med en molekylvikt mindre än 1000 Da) utövar effektiva terapeutiska effekter genom att finmodulera proteinaktiviteter, överflöd och interaktioner. Vanliga läkemedel med små molekyler inkluderar naturliga produkter och deras derivat (t.ex. växtbaserade monomerer) såväl som kemiskt syntetiserade läkemedel. När de kommer in i människokroppen utövar dessa läkemedel sina terapeutiska effekter genom att binda till målproteiner i celler eller externt. Att förstå hur småmolekylära läkemedel binder till målproteiner är därför särskilt avgörande vid läkemedelsutveckling, särskilt i komplexa fysiologiska miljöer som levande celler, blod och sjuka vävnader. En djupgående analys av interaktionen mellan småmolekylära läkemedel och proteiner möjliggör inte bara exakt identifiering av läkemedelsmål utan avslöjar också de molekylära mekanismerna för läkemedelsverkan och potentiella effekter utanför målet. Dessutom har det löftet att upptäcka nya terapeutiska mål, och därigenom tillhandahålla rikare strategier för sjukdomsbehandling.
Förutom småmolekylära läkemedel deltar endogena småmolekylära metaboliter i organismer, såsom ATP, kolesterol, gallsyror, arakidonsyra och retinsyra, i att reglera många viktiga signalvägar och proteinaktiviteter genom att interagera med proteiner, inklusive transportproteiner, membran. receptorer, transkriptionsfaktorer och metaboliska enzymer. Under de senaste åren har interaktionen mellan metaboliter i tarmmikrobiota och värdceller dykt upp som en forskningshotspot. Därför är grundlig undersökning och kartläggning av interaktionsnätverken mellan metaboliter och proteiner i cellulära miljöer, särskilt under sjukdomstillstånd, av stor betydelse för att förstå livsprocesser och behandla sjukdomar.
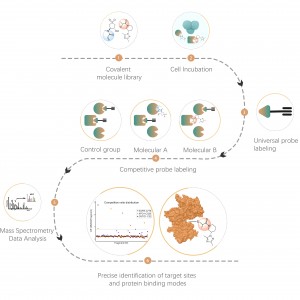
Kemisk proteomik, som en betydande gren av kemisk biologi, har nu använts i stor utsträckning inom proteinfunktionsforskning, identifiering av småmolekylära läkemedelsmål och screening av nya läkemedelsstrukturer. Denna tekniska plattform använder en mängd olika funktionellt olika kemiska sonder, kombinerade med proteomik, som syftar till att belysa interaktionsmekanismerna mellan små molekyler och proteiner under fysiologiska förhållanden (såsom levande celler, blod, vävnader, etc.). Det är värt att nämna att, jämfört med renade proteinsystem, är användningen av levande cellsystem en viktig egenskap hos kemisk proteomik. Det möjliggör en realistisk skildring av fördelningen av mål för småmolekylära läkemedel, endogena metaboliter, etc., inom komplexa proteomer, även ner till nivån av aminosyrarester.
Chomix erbjuder professionella analystjänster för interaktioner mellan små molekyler och proteiner, vilket ger dig möjlighet att fördjupa dig i potentiella läkemedelsmål och förbättra din förståelse för läkemedels molekylära mekanismer och potentiella biverkningar. Vårt expertteam har lång erfarenhet av kemisk proteomikforskning och kommer att välja de mest lämpliga och pålitliga metoderna åt dig, vilket eliminerar alla farhågor om tekniska utmaningar och underlättar utvecklingen av din forskning utan ansträngning.

Teknisk service
1. Identifiering av direkta mål för icke-kovalenta småmolekylära läkemedel
De flesta småmolekylära läkemedel interagerar med målproteiner genom icke-kovalent bindning, bildar dynamiska och reversibla interaktioner med aminosyrarester i bindningsfickor via vätebindningar, π-π-stapling, hydrofoba interaktioner etc. Därför stabil anrikning och isolering av proteiner bundna av icke-kovalenta småmolekylära läkemedel från komplexa proteomer utgör betydande utmaningar. För att komma till rätta med detta har Chomix utvecklat en plattform för identifiering av kemiska proteomikmål baserad på fotosonder. Denna plattform fångar exakt den dynamiska bindningen mellan små molekyler och proteiner i levande celler och uppnår separation och anrikning, och identifierar därigenom övergripande direkta mål för icke-kovalenta småmolekylära läkemedel på proteomisk nivå.
2. Identifiering av bindningsfickor för icke-kovalenta småmolekylära läkemedel
I processen för utveckling av småmolekylära läkemedel är det avgörande att först fastställa bindningsinformationen mellan läkemedlet och proteinet, och sedan specificera vilken speciell ficka på proteinytan läkemedlet binder till och hur det binder. Denna information är väsentlig för efterföljande läkemedelsstrukturoptimering. Förutom klassiska strukturbiologiska tillvägagångssätt har Chomix också utvecklat en avancerad kemisk proteomikteknologiplattform baserad på högupplöst masspektrometri. Denna plattform kan identifiera bindande peptider för icke-kovalenta småmolekylära läkemedel på proteinnivå och till och med cellulär nivå, och därigenom hjälpa till att ta itu med denna kritiska fråga i tidig läkemedelsutveckling.
3. Kvantitativ analys av beläggning och selektivitet för kovalenta småmolekylära läkemedelsmål
Kovalenta läkemedel avser läkemedel som bildar stabila kovalenta bindningar med aminosyrarester vid bindningsfickor på målproteiner, såsom de som binder till cystein, lysin, serin, etc. Vanliga kovalenta läkemedel inkluderar aspirin, osimertinib, zebularin, såväl som naturliga produkter som t.ex. artemisinin och artesunat. I levande celler kan kovalenta läkemedel stabilt binda till och uppta specifika aminosyrarester på målproteiner. Genom att utnyttja denna egenskap har Chomix framgångsrikt utvecklat en kemisk proteomikplattform baserad på en universell sond. Denna plattform möjliggör kvantitativ analys av beläggning av målställen för kovalenta småmolekylära läkemedel, ner till nivån av aminosyrarester. Dessutom, genom att analysera beläggningsinformation för över 10 000 aminosyrarester, kan den bestämma målselektivitet vid olika läkemedelskoncentrationer, vilket ger kraftfull vägledning för tidig läkemedelsutveckling.
4. Identifiering och selektivitetsanalys av proteinnedbrytande mål
Som en ny typ av läkemedel skiljer sig Proteolysis Targeting Chimeras (PROTAC) från traditionella småmolekylära hämmare eller aktivatorer. De undergräver det konventionella "beläggningsdrivna" utvecklingskonceptet inom medicinsk kemi genom att använda det endogena ubiquitin-proteasomsystemet (UPS) för att specifikt bryta ned sjukdomsframkallande proteiner, särskilt de som anses vara "odugliga" mål. Därför är kvantitativ identifiering av proteinnedbrytande läkemedelsmål och deras selektivitet på hela proteomnivån avgörande för tidig utveckling av sådana läkemedel. Chomix har framgångsrikt utvecklat olika kvantitativa teknologiplattformar för kemisk proteomik som kan kvalitativt och kvantitativt analysera över 5 000 proteiner i individuella cellinjer, vilket ger en omfattande och djupgående analys av målselektivitet.